
-
中文 | EN

中文 | EN
发布时间:2025-06-03 00:00:00.0
哺乳动物体内的游离脂肪酸种类丰富,既是重要的能量来源,也是脂质合成的前体和关键信号分子,在维持机体代谢稳态中发挥着重要作用。脂肪酸的合成与在不同组织间的分配过程受到精密调控,其失衡可能破坏脂质代谢稳态,诱发非酒精性脂肪肝、肥胖和胰岛素抵抗等代谢相关疾病。然而,目前对于哺乳动物体内脂肪酸的组织特异性合成以及其在组织间的转运交流仍缺乏系统性认识。
近日,中国科学院上海有机化学研究所生物与化学交叉研究中心朱正江研究员团队在Advanced Science期刊发表题为 “Unraveling tissue-specific fatty acid biosynthesis and inter-tissue crosstalk in mice through stable-isotope tracing metabolomics” 的研究论文(Advanced Science, 2025, e03662)。该工作利用稳定同位素示踪代谢组学技术,系统性地揭示了小鼠体内脂肪酸的组织特异性生物合成模式及其在各组织间的代谢交流。

研究团队使用了一种非侵入性体内稳定同位素示踪代谢组学方法,通过在膳食中添加[U-13C]-葡萄糖,结合课题组自主研发的MetTracer代谢组学技术,全面描绘了13种游离脂肪酸在15种组织中的合成与分布。研究首先阐明了新生脂肪酸在不同组织中的累积差异,并结合通量分析量化了脂肪酸的组织特异性合成速率,描绘出膳食摄入后脂肪酸在多个组织中的合成时空图谱。结果显示,进食状态下脂肪组织通过快速合成脂肪酸缓冲膳食葡萄糖,而其他组织中脂肪酸的积累相对缓慢。进一步分析不同组织的脂肪酸组成特征发现,棕榈油酸是外周组织主要合成的脂肪酸,而相比之下,大脑则更倾向于合成多不饱和脂肪酸(PUFAs)及棕榈酸。此外,不同脑区之间表现出显著的脂肪酸代谢异质性:中脑、小脑和嗅球的合成速率高于海马体、皮质和脑桥,反映了脑区间在脂肪酸合成与利用方面的功能差异(图1)。
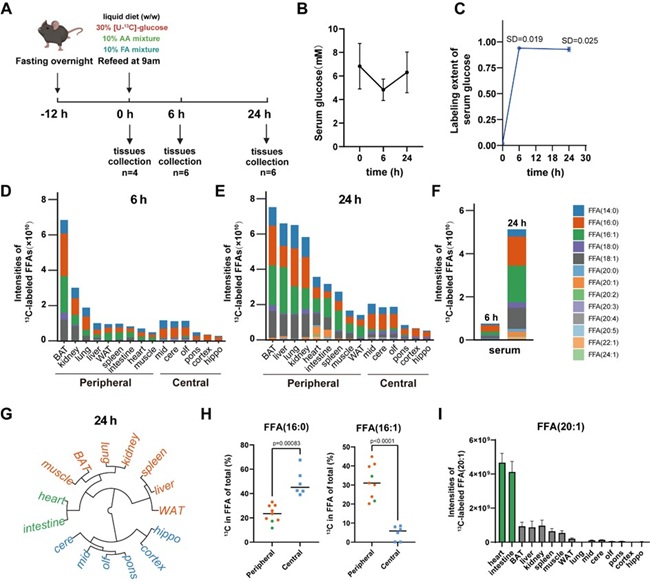
图1. 稳定同位素示踪代谢组学技术揭示脂肪酸合成代谢组织间异质性
进一步分析发现,循环系统中新合成的四种主要脂肪酸(棕榈酸、硬脂酸、棕榈油酸和油酸)主要来源于肝脏,提示禁食-恢复进食状态下血清游离脂肪酸的供应重心从脂肪组织转向肝脏。与此同时,研究还观察到不同类型脂肪酸在组织与循环系统之间的代谢串扰模式存在明显差异,多不饱和脂肪酸(PUFAs)在组织与循环系统之间展现出更为密切的代谢交流,而长链单不饱和脂肪酸(MUFAs)则相对较弱。研究通过同素体分布解卷积分析进一步定量了肝源性脂肪酸在其他组织中的贡献,发现肺和心脏等组织中超过一半的新生棕榈酸和硬脂酸源自肝脏,而棕色脂肪组织和小肠中的脂肪酸主要为自身合成(图2)。此外,该工作还探究了衰老对脂肪酸合成能力的影响。随着年龄的增长,外周组织中脂肪酸的合成能力显著下降,尤其是对MUFAs和棕榈酸的合成能力受损最为明显。相比之下,脑组织的合成能力在衰老过程中保持相对稳定,受到的影响较小,提示不同组织在应对衰老过程中存在差异化的代谢适应能力。
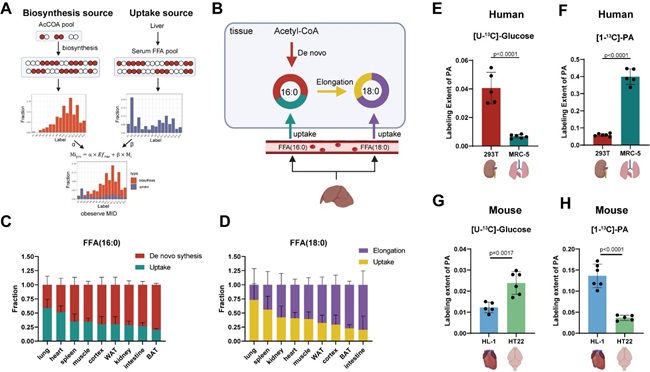
图2. 定量分析肝脏与其他组织的脂肪酸代谢交流
综上,该研究构建了一套系统的脂肪酸代谢示踪分析方法,首次在模式动物小鼠全身层面定量解析了脂肪酸的组织特异性合成与跨组织转运,为理解膳食碳源利用、脂肪酸合成及代谢稳态调控提供了新的视角和重要数据支撑。
中国科学院上海有机化学研究所生物与化学交叉研究中心博士研究生邢倍滋为论文第一作者,朱正江研究员为论文的通讯作者。中国科学院上海有机化学研究所生物与化学交叉研究中心为第一单位。该工作得到了国家自然科学基金委、科技部、中国科学院、上海市科委等的资助。
论文链接:https://doi.org/10.1002/advs.202503662
